- 1.43 MB
- 2022-07-30 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
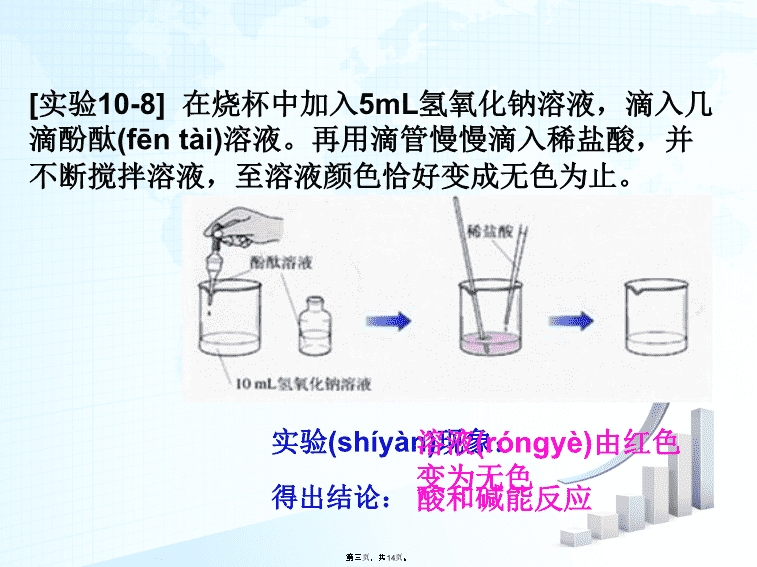
酸碱中和反应(fǎnyìng)第一页,共14页。\n1、为什么酸和碱都有相似的化学性质(huàxuéxìngzhì)?2、判断下列物质哪些是酸?哪些是碱?H2SO4、Fe(OH)3、Al(OH)3、HNO3、KOH、NH3·H2O、CH3COOH、HCl、H3PO4知识(zhīshi)回顾思考:酸和碱能否(nénɡfǒu)发生化学反应?第二页,共14页。\n[实验10-8]在烧杯中加入5mL氢氧化钠溶液,滴入几滴酚酞(fēntài)溶液。再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。实验(shíyàn)现象:溶液(róngyè)由红色变为无色得出结论:酸和碱能反应第三页,共14页。\nNaOH+HCl=NaCl+H2ONaOH和HCl反应(fǎnyìng)的方程式酸溶液中的H+和碱溶液中的OH-反应生成(shēnɡchénɡ)水,剩下的金属离子和酸根离子结合生成(shēnɡchénɡ)盐的过程。反应(fǎnyìng)本质:第四页,共14页。\n中和反应(fǎnyìng)定义:酸与碱作用,生成盐和水的反应(fǎnyìng),叫做中和反应(fǎnyìng)如:Ca(OH)2+2HCl=CaCl2+2H2O2NaOH+H2SO4=Na2SO4+2H2O第五页,共14页。\nKOH+H2SO4Mg(OH)2+HClAl(OH)3+H2SO4Cu(OH)2+HClK2SO4+2H2OMgCl2+2H2OAl2(SO4)3+6H2OCuCl2+2H2O22练习:完成(wánchéng)下列化学方程式:232第六页,共14页。\nCa(OH)2H2SO4CaSO42H2O+=+熟石灰你能用方程式表达出它的原理么?(说明:此酸雨为硫酸型酸雨)中和反应(fǎnyìng)在日常生活中的应用1.改变(gǎibiàn)土壤的酸碱性第七页,共14页。\n方法(fāngfǎ)1:可用熟石灰进行中和处理。处理方法2:在废硫酸(liúsuān)中加入废铁(硫酸(liúsuān)亚铁可用来做动物的食品添加剂。)2.处理工厂(gōngchǎng)的废水第八页,共14页。\n试写出胃康—U治胃酸过多的原理(yuánlǐ):此药中含有(hányǒu)氢氧化铝3HCl+Al(OH)3=AlCl3+3H2O3.用于医药(yīyào)第九页,共14页。\n思考:为什么被蚊虫叮咬过之后会觉得痛痒?有什么办法能消除肿痛?思考:为什么吃碱面时,放点醋,味道会更美?第十页,共14页。\n溶液(róngyè)酸碱度的表示法酸性(suānxìnɡ)溶液的pH值<7碱性(jiǎnxìnɡ)溶液的pH值>7中性溶液的pH值=7酸性越强,pH越小碱性越强,pH越大(NaCl溶液、Na2SO4溶液)(p小写,H大写)第十一页,共14页。\n测定溶液(róngyè)pH的最简便方法—使用pH试纸在白瓷板或玻璃片上放一小片pH试纸,将被测液滴到试纸上,把试纸显示(xiǎnshì)的颜色与标准比色卡比较,即可得出被测液的pH.①不能将pH试纸直接(zhíjiē)浸入待测液中测定,否则待测液受到污染。②不能先用蒸馏水将pH试纸润湿,否则待测液被稀释,测出的pH不准确。第十二页,共14页。\n1.下列(xiàliè)反应中属于中和反应的是()A、Zn+2HCl=ZnCl2+H2↑B、CuO+2HCl=CuCl2+H2OC、Ba(OH)2+H2SO4=BaSO4↓+2H2OD、AgNO3+HCl=AgCl↓+HNO3C2.下列各组物质(wùzhì)通常借助指示剂才能证明是否反应的是()A、氢氧化铜和稀盐酸B、石灰石和稀盐酸C、氢氧化钙与碳酸钠反应D、烧碱和稀硫酸请同学(tóngxué)们试一下D第十三页,共14页。\n3.已知苹果汁的近似pH值为2.9~3.3,在苹果汁中滴入紫色石蕊试液(shìyè),显示的颜色是()(A)无色(B)红色(C)蓝色(D)紫色B4.下列各pH值表示溶液(róngyè)酸性最强的是()(A)pH=14(B)pH=7(C)pH=1(D)pH=0D5.将一定溶质质量分数的氢氧化钠溶液加水稀释,下图中能正确(zhèngquè)表示pH变化的是()A第十四页,共14页。