- 1.29 MB
- 2022-03-30 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第四节玻尔的原子模型课堂探究探究一玻尔理论的理解问题导引丹麦物理学家玻尔意识到了经典理论在解释原子结构方面的困难。在普朗克关于黑体辐射的量子理论和爱因斯坦关于光子的概念的启发下,他在1913年把微观世界中物理量取分立值得观念应用到原子系统。那么在玻尔的头脑中,原子模型会是一幅什么图景呢?玻尔提示:原子中的电子绕原子核做匀速圆周运动,服从经典力学规律,但轨道是量子化的,能量也是量子化的。名师精讲玻尔的原子模型的主要内容1.轨道量子化:轨道半径只能够是一些不连续的、某些分立的数值。氢原子各条可能轨道上的半径rn=n2r1(n=1,2,3,…)其中n是正整数,r1是离核最近的可能轨道的半径,r1=0.53×10-10m。其余可能的轨道半径还有0.212nm、0.477nm……不可能出现介于这些轨道半径之间的其他值。这样的轨道形式称为轨道量子化。2.能量量子化:(1)电子在可能轨道上运动时,尽管是变速运动,但它并不释放能量,原子是稳定的,这样的状态也称之为定态。(2)由于原子的可能状态(定态)是不连续的,具有的能量也是不连续的。这样的能量值,称为能级,能量最低的状态称为基态,其他的状态叫作激发态,对氢原子,以无穷远处为势能零点时,其能级公式En=E1(n=1,2,3,…)其中E1代表氢原子的基态的能级,即电子在离核最近的可能轨道上运动时原子的能量值,E1=-13.6eV。n是正整数,称为量子数。量子数n越大,表示能级越高。(3)原子的能量:En=Ekn+Epn,即原子的能量包括:原子的原子核与电子所具有的电势能和电子运动的动能。当氢原子中的电子绕核运动时:=,故Ekn=mv2=
。当电子的轨道半径增大时,库仑引力做负功,原子的电势能增大,动能减小;反之电势能减小,动能增大。与卫星绕地球运行相似。3.跃迁:原子从一种定态(设能量为E2)跃迁到另一种定态(设能量为E1)时,它辐射(或吸收)一定频率的光子,光子的能量由这两种定态的能量差决定,即高能级Em低能级En。可见,电子如果从一个轨道到另一个轨道,不是以螺旋线的形式改变半径大小的,而是从一个轨道上“跳跃”到另一个轨道上。玻尔将这种现象叫作电子的跃迁。警示(1)处于基态的原子是稳定的,而处于激发态的原子是不稳定的。(2)原子的能量与电子的轨道半径相对应,轨道半径大,原子的能量大,轨道半径小,原子的能量小。【例题1】已知氢原子的基态能量为-13.6eV,核外电子的第一轨道半径为0.53×10-10m,电子质量me=9.1×10-31kg,电荷量为1.6×10-19C,求电子跃迁到第三轨道时,氢原子的能量、电子的动能各多大?点拨:原子的能量应根据能级进行计算。解析:氢原子的能量可由氢原子能级公式En=E1求出,而动能可由氢原子轨道半径公式以及向心力公式求出。氢原子的能量为电子的动能和电势能之和,则第三个问题不难求出。氢原子的能量为E3=E1=-1.51eV电子在第三轨道时半径为r3=n2r1=32r1=9r1①电子绕核做圆周运动,向心力由库仑力提供,所以=②由①②可得电子的动能为:Ek3=mev==eV=1.51eV答案:-1.51eV 1.51eV反思求解电子在某条轨道上的运动动能时,要将玻尔的轨道理论与电子绕核做圆周运动的向心力结合起来。即F向=,F向=F库=探究二氢原子的能级结构和跃迁问题的理解
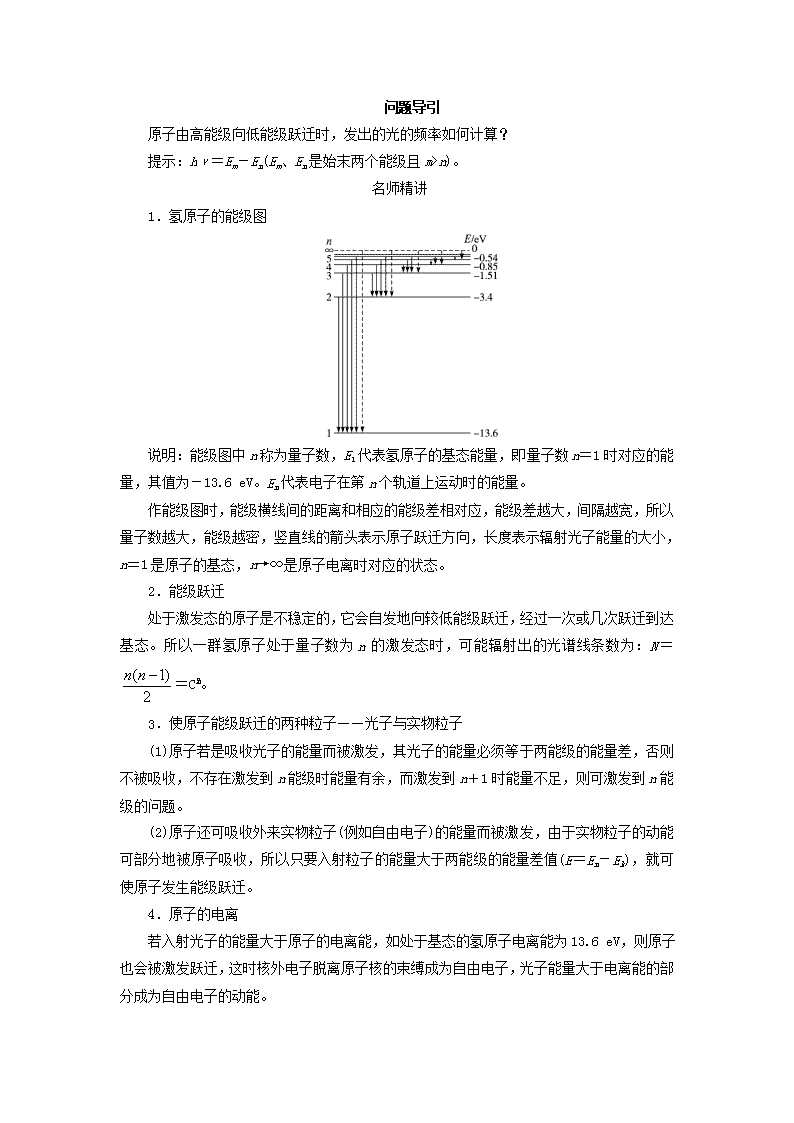
问题导引原子由高能级向低能级跃迁时,发出的光的频率如何计算?提示:hν=Em-En(Em、En是始末两个能级且m>n)。名师精讲1.氢原子的能级图说明:能级图中n称为量子数,E1代表氢原子的基态能量,即量子数n=1时对应的能量,其值为-13.6eV。En代表电子在第n个轨道上运动时的能量。作能级图时,能级横线间的距离和相应的能级差相对应,能级差越大,间隔越宽,所以量子数越大,能级越密,竖直线的箭头表示原子跃迁方向,长度表示辐射光子能量的大小,n=1是原子的基态,n→∞是原子电离时对应的状态。2.能级跃迁处于激发态的原子是不稳定的,它会自发地向较低能级跃迁,经过一次或几次跃迁到达基态。所以一群氢原子处于量子数为n的激发态时,可能辐射出的光谱线条数为:N==C。3.使原子能级跃迁的两种粒子——光子与实物粒子(1)原子若是吸收光子的能量而被激发,其光子的能量必须等于两能级的能量差,否则不被吸收,不存在激发到n能级时能量有余,而激发到n+1时能量不足,则可激发到n能级的问题。(2)原子还可吸收外来实物粒子(例如自由电子)的能量而被激发,由于实物粒子的动能可部分地被原子吸收,所以只要入射粒子的能量大于两能级的能量差值(E=En-Ek),就可使原子发生能级跃迁。4.原子的电离若入射光子的能量大于原子的电离能,如处于基态的氢原子电离能为13.6eV,则原子也会被激发跃迁,这时核外电子脱离原子核的束缚成为自由电子,光子能量大于电离能的部分成为自由电子的动能。
百度文库-让每个人平等地提升自我警示(1)当一个氢原子从某一轨道向另一个轨道跃迁时,可能的情况只有一种,但大量的氢原子就会出现多种情况。(2)使处于基态或激发态的原子的核外电子跃迁到无穷远时,称为电离,所需能量称为电离能。【例题2】有一群氢原子处于量子数n=4的激发态,当它们跃迁时:(1)有可能放出几种能量的光子?(2)在哪两个能级间跃迁时,所发出的光子的波长最长?波长是多少?点拨:本题中氢原子在n=4的定态,原子处于激发态,电子可能从n=4轨道向低轨道跃迁,向外以光子形式辐射能量,辐射的光子能量hν等于两定态能级的能量差,可放出C种频率的光子。由hν=ΔE知λ=,波长最长的光子对应的ΔE最小。解析:(1)一群处于量子数n=4的激发态的氢原子向低能级跃迁能放出的光子数为N===6(种)。(2)由hν=Em-En和ν=,可得λ=,由n=4向n=3跃迁能级差最小,光子的波长最长ΔE=-0.85eV-(-1.51eV)=0.66eV,代入数值得λ=m=1.88×10-6m。答案:(1)6 (2)n=4向n=3的跃迁 1.88×10-6m反思氢原子从高能级向低能级跃迁时,对一个氢原子来说,可能辐射(n-1)种频率的光子;对一群氢原子而言,则可能辐射种频率的光子。光子的波长和频率可用hν=ΔE和=ΔE求解。触类旁通在例题2中,有一个氢原子处于量子数n=3的激发态,当它跃迁时,有可能放出几种频率的光子?答案:2种