- 1.03 MB
- 2021-05-22 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
1
六安一中 2020 届高三年级适应性考试
理科综合试题
第 I 卷(选择题 共 126 分)
可能用到的相对原子质量:N 14 O 16 Cl 35.5
一、选择题:本题共 13 小题,每小题 6 分,在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.下列有关细胞中元素和化合物的叙述正确的是( )
A.淀粉、纤维素、糖原不同的原因是组成其基本单位的排列顺序不同
B.组成 DNA 和 RNA 的元素种类不同,含氮碱基也不完全相同
C.氨基酸脱水缩合形成多肽时,生成的水中的氧来源于氨基酸的羧基
D.等质量的脂肪和糖类氧化分解,脂肪释放能量多,脂肪是主要的能源物质
2.基因型为 AaBb(两对基因独立遗传)的某二倍体生物有以下几种细胞分裂图像,下列说法
正确的是( )
A.甲图中基因 a 最可能来源于染色体的交叉互换
B.乙图中基因 a 不可能来源于基因突变
C.丙产生的子细胞发生的变异属于染色体结构变异
D.丁图中基因 a 的出现最可能与基因重组有关
3.如图为人体某致病基因控制异常蛋白质合成过程
的示意图。据图分析错误的是( )
A.过程①表示转录,以一条链为模板,以脱氧核
苷酸为原料
B.过程②表示翻译,图中核糖体的移动方向是自
右向左
C.异常多肽中丝氨酸的反密码子为 AGA,则物
质 a 模板链相应碱基为 AGA
D.图中基因控制合成的蛋白质,可能导致膜功能
的改变
4.(2019•福建高三开学考试)黄色小鼠(AA)与黑色小鼠(aa)杂交,产生的 F1(Aa)不同
个体出现了不同体色。研究表明,不同体色的小鼠 A 基因的碱基序列相同,但 A 基因中二
核苷酸(CpG)的胞嘧啶有不同程度的甲基化(如图),
而甲基化不影响 DNA 复制。下列有关分析错误的是
( )
A.F1 个体体色的差异可能与 A 基因甲基化程度有关
B.碱基甲基化可能影响 RNA 聚合酶与该基因的结合
C.碱基甲基化不影响遗传信息的传递
D.A 基因中的碱基甲基化引起了基因突变
5.(2020•湖北省高三期末)某同学将三组含有不同浓度(C1、C2 和 C3 三种;均达不到抑制
胚芽鞘生长浓度)生长素的琼脂块分别放置在去顶胚芽鞘左侧,一段时间后测量并记录弯
曲角度(与右侧水平面夹角)的值分别为α1、α2 和α3。若三组琼脂块所含生长素浓度关系
为 C1>C2>C3,则实验结果对应的弯曲角度关系不可能为( )
A.α1>α2>α3 B.α3>α1>α2 C.α1>α3>α2 D.α2>α1>α3
6.垃圾分类收集处理具有重要意义,下列有关垃圾分类的说法错误的是
A.可回收垃圾收集处理可以实现物质的循环利用,减少废弃物污染,保护生态环境
B.厨余垃圾中剩饭、剩菜所含的有机物经发酵处理后可以实现能量的循环利用
C.有害垃圾中对人体有害的重金属、有毒物质处理不合理时可以通过食物链进入到人体中
D.其他垃圾采取卫生填埋可有效减少对地下水、地表水、土壤及空气的污染
7.化学与人类社会的生产、生活有着密切联系,下列叙述正确的是( )
A.新型冠状病毒对高三学子的复习备考造成了一定的挑战,质量分数 0.5%的过氧乙酸溶
液能高效杀死该病毒,在重症隔离病房用过氧乙酸与苯酚溶液混合可以提高消杀效率
B.5G 技术联通世界离不开光缆,光缆的主要成分是晶体硅
C.乙醚与乙醇互为同分异构体
D.古代侍者为防止气息传到皇帝的食物上使用丝巾做成口罩遮盖口鼻,丝巾的主要成分是
蛋白质
8.已知 NA 是阿伏加德罗常数的值,下列说法正确..的是( )
A.4.6g14CO2 与 N218O 的混合物中所含中子数为 2.4NA
B.密闭容器中,2 mol NO 和 1 mol O2 反应后分子总数为 2NA
C.44.0 g 环氧乙烷中含有 7.0 NA 个极性键
D.标准状况下,2.24 L 三氯甲烷中含碳氯共价键的数目为 0.3 AN
9.某黄酮类药物的合成涉及反应 下列说法正确的是( )
A.化合物 X 在空气中能稳定存在
B.化合物 X 中所有碳原子可处于同一平面
C.化合物 X、Y 都可与溴水发生加成反应
2
D.1mol 化合物 Y 最多可以与 4molH2 反应
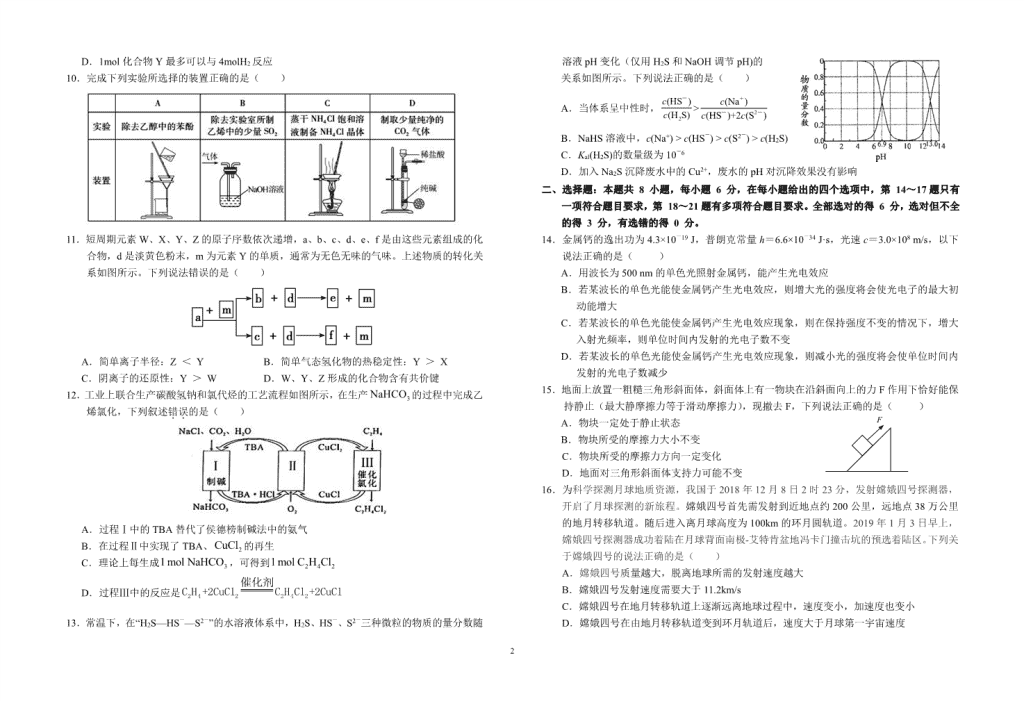
10.完成下列实验所选择的装置正确的是( )
11.短周期元素 W、X、Y、Z 的原子序数依次递增,a、b、c、d、e、f 是由这些元素组成的化
合物,d 是淡黄色粉末,m 为元素 Y 的单质,通常为无色无味的气味。上述物质的转化关
系如图所示。下列说法错误的是( )
A.简单离子半径:Z < Y B.简单气态氢化物的热稳定性:Y > X
C.阴离子的还原性:Y > W D.W、Y、Z 形成的化合物含有共价键
12.工业上联合生产碳酸氢钠和氯代烃的工艺流程如图所示,在生产 3NaHCO 的过程中完成乙
烯氯化,下列叙述错误..的是( )
A.过程Ⅰ中的 TBA 替代了侯德榜制碱法中的氨气
B.在过程Ⅱ中实现了 TBA、 2CuCl 的再生
C.理论上每生成 31mol NaHCO ,可得到 2 4 21mol C H Cl
D.过程Ⅲ中的反应是 2 4 2 2 4 2
催化剂
C H +2CuCl C H Cl +2CuCl
13.常温下,在“H2S—HS-—S2-”的水溶液体系中,H2S、HS-、S2-三种微粒的物质的量分数随
溶液 pH 变化(仅用 H2S 和 NaOH 调节 pH)的
关系如图所示。下列说法正确的是( )
A.当体系呈中性时,
2
(HS )
(H S)
c
c
-
>
+
2
(Na )
(HS )+2 (S )
c
c c- -
B.NaHS 溶液中,c(Na+) > c(HS-) > c(S2-) > c(H2S)
C.Kal(H2S)的数量级为 10-6
D.加入 Na2S 沉降废水中的 Cu2+,废水的 pH 对沉降效果没有影响
二、选择题:本题共 8 小题,每小题 6 分,在每小题给出的四个选项中,第 14~17 题只有
一项符合题目要求,第 18~21 题有多项符合题目要求。全部选对的得 6 分,选对但不全
的得 3 分,有选错的得 0 分。
14.金属钙的逸出功为 4.3×10-19 J,普朗克常量 h=6.6×10-34 J·s,光速 c=3.0×108 m/s,以下
说法正确的是( )
A.用波长为 500 nm 的单色光照射金属钙,能产生光电效应
B.若某波长的单色光能使金属钙产生光电效应,则增大光的强度将会使光电子的最大初
动能增大
C.若某波长的单色光能使金属钙产生光电效应现象,则在保持强度不变的情况下,增大
入射光频率,则单位时间内发射的光电子数不变
D.若某波长的单色光能使金属钙产生光电效应现象,则减小光的强度将会使单位时间内
发射的光电子数减少
15.地面上放置一粗糙三角形斜面体,斜面体上有一物块在沿斜面向上的力 F 作用下恰好能保
持静止(最大静摩擦力等于滑动摩擦力),现撤去 F,下列说法正确的是( )
A.物块一定处于静止状态
B.物块所受的摩擦力大小不变
C.物块所受的摩擦力方向一定变化
D.地面对三角形斜面体支持力可能不变
16.为科学探测月球地质资源,我国于 2018 年 12 月 8 日 2 时 23 分,发射嫦娥四号探测器,
开启了月球探测的新旅程。嫦娥四号首先需发射到近地点约 200 公里,远地点 38 万公里
的地月转移轨道。随后进入离月球高度为 100km 的环月圆轨道。2019 年 1 月 3 日早上,
嫦娥四号探测器成功着陆在月球背面南极-艾特肯盆地冯卡门撞击坑的预选着陆区。下列关
于嫦娥四号的说法正确的是( )
A.嫦娥四号质量越大,脱离地球所需的发射速度越大
B.嫦娥四号发射速度需要大于 11.2km/s
C.嫦娥四号在地月转移轨道上逐渐远离地球过程中,速度变小,加速度也变小
D.嫦娥四号在由地月转移轨道变到环月轨道后,速度大于月球第一宇宙速度
F
3
A
V a
b R2
R1
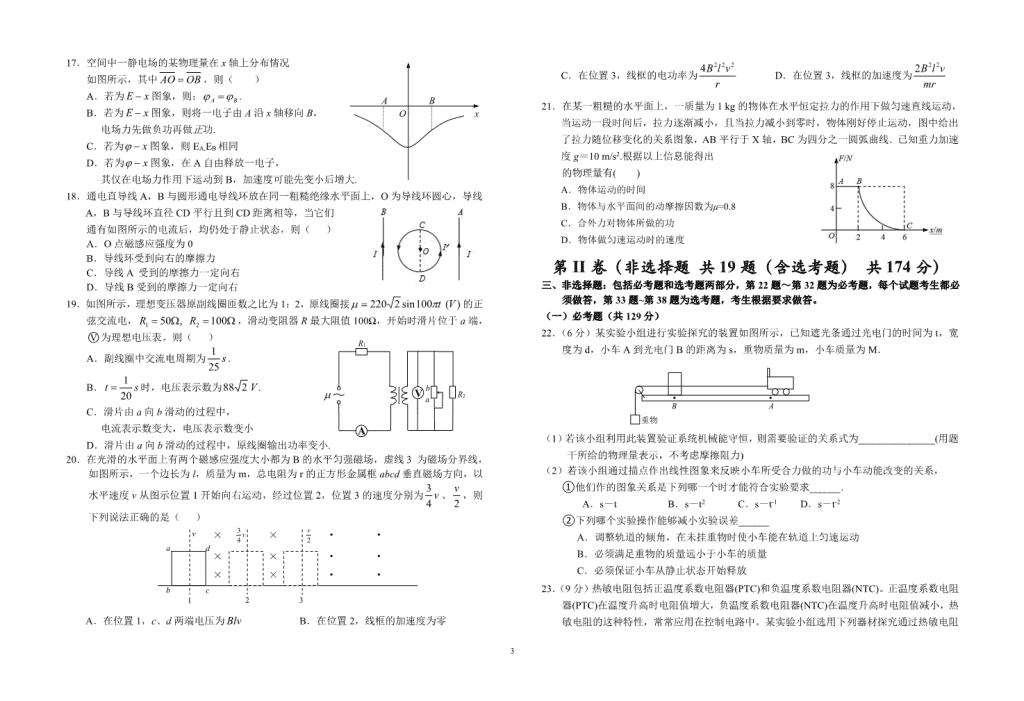
17.空间中一静电场的某物理量在 x 轴上分布情况
如图所示,其中 OBAO ,则( )
A.若为 xE 图象,则: BA .
B.若为 xE 图象,则将一电子由 A 沿 x 轴移向 B,
电场力先做负功再做正功.
C.若为 x 图象,则 EA,EB 相同
D.若为 x 图象,在 A 自由释放一电子,
其仅在电场力作用下运动到 B,加速度可能先变小后增大.
18.通电直导线 A,B 与圆形通电导线环放在同一粗糙绝缘水平面上,O 为导线环圆心,导线
A,B 与导线环直径 CD 平行且到 CD 距离相等,当它们
通有如图所示的电流后,均仍处于静止状态,则( )
A.O 点磁感应强度为 0
B.导线环受到向右的摩擦力
C.导线 A 受到的摩擦力一定向右
D.导线 B 受到的摩擦力一定向右
19.如图所示,理想变压器原副线圈匝数之比为 1:2,原线圈接 )(100sin2220 Vt 的正
弦交流电, 100,50 21 RR ,滑动变阻器 R 最大阻值 100Ω,开始时滑片位于 a 端,
○V 为理想电压表。则( )
A.副线圈中交流电周期为 s25
1 .
B. st 20
1 时,电压表示数为 .288 V
C.滑片由 a 向 b 滑动的过程中,
电流表示数变大,电压表示数变小
D.滑片由 a 向 b 滑动的过程中,原线圈输出功率变小.
20.在光滑的水平面上有两个磁感应强度大小都为 B 的水平匀强磁场,虚线 3 为磁场分界线,
如图所示,一个边长为 l,质量为 m,总电阻为 r 的正方形金属框 abcd 垂直磁场方向,以
水平速度 v 从图示位置 1 开始向右运动,经过位置 2,位置 3 的速度分别为 v4
3 、
2
v ,则
下列说法正确的是( )
A.在位置 1,c、d 两端电压为 Blv B.在位置 2,线框的加速度为零
C.在位置 3,线框的电功率为
r
vlB 2224 D.在位置 3,线框的加速度为
mr
vlB 222
21.在某一粗糙的水平面上,一质量为 1 kg 的物体在水平恒定拉力的作用下做匀速直线运动,
当运动一段时间后,拉力逐渐减小,且当拉力减小到零时,物体刚好停止运动,图中给出
了拉力随位移变化的关系图象,AB 平行于 X 轴,BC 为四分之一圆弧曲线.已知重力加速
度 g=10 m/s2.根据以上信息能得出
的物理量有( )
A.物体运动的时间
B.物体与水平面间的动摩擦因数为μ=0.8
C.合外力对物体所做的功
D.物体做匀速运动时的速度
第 II 卷(非选择题 共 19 题(含选考题) 共 174 分)
三、非选择题:包括必考题和选考题两部分,第 22 题~第 32 题为必考题,每个试题考生都必
须做答,第 33 题~第 38 题为选考题,考生根据要求做答。
(一)必考题(共 129 分)
22.(6 分)某实验小组进行实验探究的装置如图所示,已知遮光条通过光电门的时间为 t,宽
度为 d,小车 A 到光电门 B 的距离为 s,重物质量为 m,小车质量为 M.
(1)若该小组利用此装置验证系统机械能守恒,则需要验证的关系式为_______________(用题
干所给的物理量表示,不考虑摩擦阻力)
(2)若该小组通过描点作出线性图象来反映小车所受合力做的功与小车动能改变的关系,
①他们作的图象关系是下列哪一个时才能符合实验要求______.
A.s-t B.s-t2 C.s-t-1 D.s-t-2
②下列哪个实验操作能够减小实验误差______
A.调整轨道的倾角,在未挂重物时使小车能在轨道上匀速运动
B.必须满足重物的质量远小于小车的质量
C.必须保证小车从静止状态开始释放
23.(9 分)热敏电阻包括正温度系数电阻器(PTC)和负温度系数电阻器(NTC)。正温度系数电阻
器(PTC)在温度升高时电阻值增大,负温度系数电阻器(NTC)在温度升高时电阻值减小,热
敏电阻的这种特性,常常应用在控制电路中。某实验小组选用下列器材探究通过热敏电阻
BA
xO
×
×
×
×
×
×
•
•
•
•
•
•
1 2 3
a
b
d
c
v v4
3
2
v
AB
重物
4
Rx(常温下阻值约为 10.0 Ω)的电流随其两端电压变化的特点。
A.电流表 A1(量程 100 mA,内阻约 1 Ω) B.电流表 A2(量程 0.6 A,内阻约 0.3 Ω)
C.电压表 V1(量程 3.0 V,内阻约 3 kΩ) D.电压表 V2(量程 15.0 V,内阻约 10 kΩ)
E.滑动变阻器 R(最大阻值为 10 Ω) F.滑动变阻器 R′(最大阻值为 500 Ω)
G.电源 E(电动势 15 V,内阻忽略) H.开关、导线若干
(1)实验中改变滑动变阻器滑片的位置,使加在热敏电阻两端的电压从零开始逐渐增大,请
在所提供的器材中选择必需的器材,应选择的器材为:电流表________;电压表________;
滑动变阻器________。(只需填写器材前面的字母即可)
(2)请在所提供的器材中选择必需的器材,在如图虚线框内画出该小组设计的电路图。
(3)该小组测出热敏电阻 R1 的 U/I 图线如图 2 曲线Ⅰ所示,请分析说明该热敏电阻是
________(填“PTC”或“NTC”)热敏电阻。
(4)该小组又通过查阅资料得出了热敏电阻 R2 的 U/I 图线如图 2 曲线Ⅱ所示。然后又将热敏
电阻 R1、R2 分别与某电池组连成电路如图 3 所示。测得通过 R1 和 R2 的电流分别为 0.30 A
和 0.60 A,则该电池组的电动势为________ V,内阻为________ Ω。(结果均保留三位有
效数字)
24.(12 分)如图所示平面内,O 为原点,第一象限内有平行于 y 轴的匀强电场,第四象限有
垂直于 xOy 平面向外的矩形匀强磁场,磁感应强度大小为 B。有一带电粒子从 y 轴上的 M
点垂直于 y 轴进入第一象限,经过电场后由 x 轴上的 N 点进入第四象限,粒子最终可返回
x 轴。已知 OM 距离为 3
2
L,ON 距离为 L,粒子初速度为 v,所带电荷量大小为+q,质
量为 m,重力不计。求
(1)电场强度的大小。
(2)能让粒子返回 x 轴的磁场最小面积.
25、(20 分)如图所示,光滑水平平台 AB 与竖直光滑半圆轨道 AC 平滑连接,C 点切线水平,
长为 L=4m 的粗糙水平传送带 BD 与平台无缝对接。质量分别为 m1=0.3kg 和 m2=1kg 两个
小物体用细绳将它们连接,中间有一被压缩的轻质弹簧,弹簧的弹性势能 Ep=19.5J,已知传送
带以 v0=1.5m/s 的速度向左匀速运动,小物体与传送带间动摩擦因数为μ=0.15.某时剪断细
绳,小物体 m1 向左运动, g 取 10m/s2.求:
(1)剪断细绳后 m1 向左运动速度大小;
(2)从小物体 m2 滑上传送带到第一次滑离传送带的过程中,为了维持传送带匀速运动,电动
机需对传送带多提供的电能 E;
(3)为了让小物体 m1 从 C 点水平飞出后落至 AB 平面的水平位移最大,竖直光滑半圆轨道 AC
的半径 R 和小物体 m1 平抛的最大水平位移 x 的大小。
26.(14 分)亚硝酰氯(NOCl)常用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一
氧化氮在常温常压下合成亚硝酰氯。
已知:①NOCl 是黄色气体,熔点:—64.5℃,沸点:—5.5℃;NOCl 遇水易反应生成
一种无氧酸和两种氮的常见氧化物;NOCl 对眼睛、皮肤和粘膜有强烈刺激性,具有类似
氯气和氮氧化物的毒作用。
②Ag2CrO4 是砖红色沉淀。
实验 1:制备原料气 NO 和 Cl2
利用如图 1 所示装置制备纯净的 NO 和 Cl2。
(1)制备纯净的 Cl2,烧瓶中反应的
化学方程式为 。
(2)制备纯净的 NO,烧瓶中盛有 Cu,装置Ⅱ中盛有
(填试剂名称);导管 A 的作用是 。
实验 2:制备 NOCl。
利用实验 1 中制得的 NO 和 Cl2 制备 NOCl,装置如图 2 所示。
x
y
M
NO
5
(3)仪器接口的连接顺序为 a→ (按气流从左到右顺序填写)。
(4)装置Ⅳ、Ⅴ除进一步干燥 NO 和 Cl2 外,另一作用是 。
(5)装置Ⅷ用于吸收尾气,NOCl 发生反应的化学方程式为 。
实验 3:测定 NOCl 的纯度
将所得亚硝酰氯(NOCl)产品 13.5g 溶于水,配成 250ml 该溶液,取出 25.00ml 该溶
液,以 K2CrO4 溶液为指示剂,用 1.0mol/LAgNO3 标准溶液滴定至终点,再重复上述实验
操作 2 次,测得三次实验消耗 AgNO3 标准溶液的平均体积为 20.00ml。
(6)达到滴定终点的现象是 。
(7)产品中亚硝酰氯(NOCl)的质量分数为 (保留两位小数)。
27.(15 分)随着各类电动工具的推广使用,各种大功率电池的使用量越来越大,对废旧电池
的资源化再利用日益重要。一种从废旧磷酸亚铁锂电池的正极材料(含 LiFePO4、石墨粉
和铝箔等)中综合回收锂元素、铁元素和磷元素等的工艺流程如图所示:
已知:
物质/溶解度(g)
/温度(℃) 20 40 60 80 100
LiOH 12.4 13.2 14.6 16.6 19.1
Li2CO3 1.33 1.17 1.01 0.85 0.72
回答下列问题:
(1)进行碱浸的生产车间要有良好的通风条件,理由是 。
(2)从料液 2 中获得高纯锂化合物所用的 Y 和适宜的温度是( )。
A.NaOH 20℃-40℃ B.NaOH 80℃-100℃
C.Na2CO3 20℃-40℃ D.Na2CO3 60℃-80℃
(3)X 可以是 O2 或另一种常用试剂,如 。当 X 是 O2、生成物中磷元素主要以
H2PO
4 形式存在时,氧化过程中发生反应的离子方程式为 。
(4)调节 pH 的过程中,若 Na2CO3 溶液加入量过多,会导致磷元素沉淀率降低,其可能的原
因是 ,当 Na2CO3 溶液加入量适当时,该过程中发
生反应的离子方程式为 。
(5)从料液 3 中获得 Na3PO4.10H2O 的操作是 、洗涤、干燥。
(6)科学家很早就提出锂-空气电池的概念,它直接使用金属锂作电极,从空气中获得 O2,和
以 LiFePO4 作电极的锂离子电池相比,增大了电池的能量密度(指标之一是单位质量电池
所储存的能量)。下图是某种锂-空气电池的装置
示意图,放电时,下列说法不正确的是( )
A.金属锂为负极
B.若隔膜被腐蚀,会影响该电池正常使用。
C.多孔碳电极上发生的电极反应为:
O2 + 2H2O + 4e- === 4OH-
D.锂-空气电池能量密度大的原因之一是转移
等量电子时,金属锂比 LiFePO4 质量大。
28.(14 分)甲烷是最简单的烃,可用来作为燃料,也是一种重要的化工原料。
(1)A.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH= -Q1 kJ/mol
B.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH= -Q2 kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=+Q2kJ/mol
D.
2
1 CH4(g)+O2(g)=
2
1 CO2(g)+H2O(l) ΔH=
2
1 Q2 kJ/mol
上述热化学方程式中的反应热能正确表示甲烷燃烧热的是 ,水的汽化热
ΔH= kJ/mol。
(2)以甲烷为原料通过以下反应可以合成甲醇:
2CH4(g)+O2(g) 2CH3OH(g) ΔH= -251.0kJ/mol
现将 2 mol CH4 (g)和 1 molO2 (g)充入密闭容器中,在不同温度和压强下进行上述反应。
实验测得平衡时甲醇的物质的量
随温度、压强的变化如图所示:
①P1 时升高温度,n(CH3OH)____(填“增大”、“减小”或“不变”);
P1 P2(填“>"、“<”或“=”);
②E、F、N 点对应的化学反应速率由大到小的顺序为_________
(用 v(E)、v(F)、v(N)表示);
③下列能提高 CH4 平衡转化率的措施是____(填序号);
a.选择高效催化剂 b.增大
)(
)(
2
4
On
cHn 投料比 c.及时分离产物
④若 F 点,n (CH3 OH) =1mol,总压强为 2.5MPa,则 To 时 F 点用分压强代替浓度表示的
平衡常数 Kp=________________。
⑤在温度为 T0,压强为 P2 时,各物质以下列量进行投料反应,达到平衡时,混合气体各
组分的百分含量与 E 点相同的是 。
A.4 mol CH4 (g)和 2 molO2 (g) B.2 mol CH4 (g)、1 molO2 (g)和 2 molCH3OH (g)
C.1 molCH3OH (g) D.1 mol CH4 (g)、1 molO2 (g)和 1 molCH3OH (g)
E.1 mol CH4 (g)、0.5 molO2 (g)和 1 molCH3OH (g)
高纯锂化合物
6
29.(14 分)小球藻是一种单细胞
的绿藻,它是生物实验室中一
种重要的实验植物。美国科学
家卡尔文等用小球藻作实验材
料,发现了有关植物光合作用
的“卡尔文循环”,卡尔文因此获
得了 1961 年诺贝尔化学奖。如
图为卡尔文循环反应示意图。
回答下列问题:
(1)由图可知,卡尔文循环可分
为三个阶段:CO2 的摄取期
(羧化阶段)、碳还原期和
RuBP 再生期,结合所学的
知识分析,其中属于暗反应
中 CO2 的固定阶段的是图
中的 CO2 的摄取期,这一
步反应的意义是把原本并
不活泼的____________分
子活化;属于暗反应中 C3 的还原阶段的是图中的__________________,该阶段所需
的 ATP 和 NADPH 来自____________________________。
(2)如图是研究人员通过实验得出的温度对草莓光合作用的影响(以测定的放氧速率为指标)。
据图分析回答:
①由图可知,适合草莓生长的最适温度是____________。该温度__________(填“是”或“不
是”或“不一定是”)草莓光合作用的最适温度,原因是________________________。
②实验测得,40℃培养条件下草莓叶肉细胞间隙的 CO2 浓度高于 35℃培养条件下,分析
主要原因是__________________________。
30.(6 分)新型冠状病毒衣壳外面包裹着脂质包膜,其上排列较宽的刺突蛋白(S 蛋白),形
状如太阳光环,其引起新型冠状病毒肺炎,部分重症患者因多脏器衰竭而死亡。回答下列
问题:
(1)研究表明,刺突蛋白(S 蛋白)与人体细胞表面的血管紧张素转化酶 2(ACE2)受体结
合,从而入侵人体细胞,说明细胞膜___________________的功能是相对的。
(2)我国对新型冠状病毒疫苗的研究已取得突破性进展,已经在健康志愿者身上进行试验。
在人身上做疫苗试验是安全的,是因为疫苗___________________。人体接种该疫苗后,
_________作为抗原刺激机体产生特异性抗体,一旦新型冠状病毒侵入机体,_________
会迅速增殖、分化,产生大量抗体。
(3)新型冠状病毒疫苗的研发过程直接越过了动物试验,其实是违背常规的。如图为将 SARS
病毒灭活疫苗接种到健康猴子体内后,抽取血清中的抗体进行测定的结果,据图判断在
接种后第_______天抗体达到峰值,在第 42 天两条曲线出现拐点的原因可能是_________
__________。
31.(10 分)果蝇的性别决定是 XY 型,性染色体上存在三个区段,红眼/白眼由一对等位基因
控制,基因用 R、r 表示,摩尔根的果蝇杂交实验如图所示,回答下列问题。
(1)判断眼色基因不在常染色体上的理由是__________________________________________。
(2)摩尔根当时是让白眼雄蝇与上图中 F1 红眼雌蝇进行测交,根据实验结果____________(填
“能”或“不能”)确定白眼基因位于Ⅰ区段上或是Ⅱ区段上。
(3)利用上述测交实验可得到白眼雌果蝇,与多只野生型(均为纯合子)红眼雄果蝇进行杂
7
交。
若子一代_______________________________________,则果蝇眼色基因位于Ⅱ区段上;
若子一代_______________________________________,则果蝇眼色基因位于Ⅰ区段上。
(4)一对直刚毛的雌雄果蝇杂交,后代中直刚毛雌蝇∶直刚毛雄蝇∶焦刚毛雌蝇=1∶2∶1,
判断控制直刚毛/焦刚毛的基因位于_____________________上。
32.(9 分)下图甲为人工湿地示意图,图乙中的Ⅰ和Ⅱ分别表示人工湿地上行池中养殖鲤鱼的
出生率和死亡率,图丙表示人工湿地生态系统中生物群落内的能量流动简图。请分析回答
问题:
(1)湿地植物属于人工湿地生态系统组成成分中的________;上行池与下行池中的湿地植物
种类不同,这体现了群落的________结构。
(2)图乙中,在________点时,鲤鱼的数量达到 K 值。生态学上调查鲤鱼种群数量常用的方
法是________。
(3)图丙中,属于消费者的是________。
(4)流经人工湿地生态系统的总能量除了图丙中统计的外,还有________中能量,按图丙所
示能量计算,在第二、三营养级之间的能量传递效率为____________。
(5)部分湿地植物可分泌一类特殊的化合物,吸引鸟类捕食害虫,这一现象体现了生态系统
的信息传递具________________有作用。
(二)选考题:共 45 分。请考生从给出的 2 道物理题、2 道化学题、2 道生物题中每科任选一
题做答,并用 2B 铅笔在答题卡上把所选题目的题号涂黑。注意所做题目的题号必须与
所涂题目的题号一致,在答题卡选答区域指定位置答题。如果多做,则每学科按所做的
第一题计分。
33.【物理——选修 3-3】(15 分)
(1)下列说法正确的是________.
A.晶体在一定的条件下可以转化为非晶体,但非晶体无法转化为晶体
B.物体的内能改变时温度不一定改变
C.某种液体的饱和汽压随温度的升高而增大,随体积的增大而减小
D.分子间引力和斥力都是随着分子间距离的减小而增大
E.空调机在制冷过程中,从室内吸收的热量少于向室外放出的热量
(2)如图所示,容器 A 和汽缸 B 都是导热的,A 放置在 127 ℃的恒温槽中,B 放置在 27 ℃的
空气中,大气压强为 p 空=1.0×105 Pa,开始时阀门 K 关闭,A 内为真空,其体积 VA=3.6
L,B 内活塞截面积 S=100 cm2、质量 m=2 kg,活塞下方充有理想气体,其体积为 VB=
6.0 L,活塞上方与大气连通,A 与 B 间连通细管体积不计,打
开阀门 K 后活塞缓慢下移至某一位置(未触及汽缸底部),不计
A 与 B 之间的热传递,取 g=10 m/s2.试求:
①活塞稳定后汽缸 B 内气体的体积;
②活塞下移过程中,活塞对汽缸 B 内气体做的功.
34.【物理—选修 3-4】(15 分)
(1)一列波沿 x 轴方向传播,某一时刻的波形如图所示.质点 A 与坐标原点 O 的水平距离为
0.6 m,波长λ=1.6 m,此时质点 A 沿 y 轴正方向振动,经过 0.1 s 第一次到达波峰处,则
下列说法中正确的是________.
A.这列波沿 x 轴正方向传播
B.这列波的周期 T=0.8 s
C.波速 v=14 m/s
D.从图示时刻开始,质点 A 经过Δt=1.6 s 运动的路程为 0.4 m
E.从图示时刻开始,质点 A 经过Δt′=0.5 s 第一次到达波谷
(2)如图甲所示是由透明材料制成的半圆柱体,一束细光束由真空沿着径向与 AB 成θ角射入,
对射出的折射光线的强度随θ角的变化进行记录,得到的关系如图乙所示,如图丙所示是
这种材料制成的器具,左侧是半径为 R 的半圆,右侧是长为 8R、高为 2R 的长方体,一
束单色光从左侧 A′点沿半径方向与长边成 37°角射入器具.已知光在真空中的传播速度为
c,求:(sin 37°=0.6,cos 37°=0.8)
①该透明材料的折射率;
②光线在器具中运动的总时间.
8
35.【化学--选修 3:物质结构与性质】(15 分)
(1)写出碳原子最外电子层的轨道表示式 。
(2)钛(Ti)是 22 号元素,它是______(选填编号)
a.主族元素 b.副族元素 c.短周期元素 d.长周期元素
(3)CS2 分子的电子式为______;其熔沸点比 CO2 高的原因是 。
(4)氟化钠溶液中,不存在的微粒间作用力是_________(填标号)。
A.离子键 B.共价键 C.金属键 D.范德华力 E.氢键
(5)金属铜单独与氨水或过氧化氢均不能反应,但可与过氧化氢和过量氨水的混合溶液反应
生成一种配位化合物,其反应的化学方程式可表示为_______________________。
(6)镁单质晶体中原子的堆积模型为六方最密堆积(如上图),它的晶胞是图中的__________
(填 a、b 或 c);配位数是__________________;紧邻的四个镁原子的中心连线构成的正
四面体几何体的体积是 2a cm3,镁单质的密度为ρ g·cm-3,已知阿伏伏德罗常数为 NA,
则镁的摩尔质量的计算式是________________。
36.[化学——选修 5:有机化学基础](15 分)
某芳香烃 X(分子式为 C7H8)是一种重要的有机化工原料,研究部门以它为初始原料设计
出如下转化关系图(部分产物、合成路线、反应条件略去)。其中 A 是一氯代物。
已知:
Ⅰ.
Ⅱ. (苯胺,易被氧化)
(1)写出:X→A 的反应条件____________;反应④的反应条件和反应试剂:____________。
(2)E 中含氧官能团的名称:____________;反应②的类型是_____________;反应②和③先
后顺序不能颠倒的原因是_____________________________________。
(3)写出反应①的化学方程式:_____________________________________。
(4) 有多种同分异构体,其中所有满足下列条件的同分异构体有 种。
①遇 FeCl3 溶液显紫色 ②能发生银镜反应 ③苯环上一氯代物只有 2 种。
(5)写出由 A 转化为 的合成路线_________________________________________。
(合成路线表示方法为:A B…… 目标产物)。
37.[生物——选修 1:生物技术实践](15 分)
由于塑料袋造成的“白色污染”早已成为地球公害,加拿大年仅16岁的高中生丹尼尔·伯德从
当地一个垃圾场获取泥土样本,将泥土样本跟聚乙烯和一些促进细菌生长的溶液混合,探
究培养液对塑料袋碎片的分解效果。结果,他发现绿脓杆菌和甲氰菊酯降解菌两种细菌分
解聚乙烯最为有效,回答下列有关问题。
(1)他从垃圾场的泥土样本中获取分解聚乙烯的细菌,是因为在寻找目的菌株时,要根据___
_______________________________________。
(2)纯化菌株常采用平板划线法,此过程所用的接种工具是________________,此接种工具
常采用________________灭菌法进行灭菌。
(3)对统计样品中细菌的数目进行计数时,常采用_____________________法进行接种。但统
计的菌落数往往比活菌的实际数目_______________,原因是________________________
______________。
(4)实验结束后,为防止造成对环境污染,对使用过的培养基的处理是___________________
________。
38.[生物——选修 3:现代生物科技专题](15 分)
在荧光素酶中加入正确的荧光素底物就可以放出荧光。荧光素酶及其合成基因在生物研究
中有着广泛的应用。请回答下列问题:
(1)荧光素酶基因可以从基因文库中获取,也可以通过________方法得到,再利用 PCR 技术
扩增即可,扩增荧光素酶基因利用的原理是__________________。
(2)在基因工程操作过程中,需要用________酶和________酶构建基因表达载体,基因表达
载体要有________,以便筛选出含有目的基因的受体细胞。
(3)荧光素酶基因也可以作为目的基因转入某些动植物细胞中表达产生荧光素酶。将目的基
因导入植物细胞,目前常用的目的基因载体是农杆菌的 Ti 质粒,目的基因需插入到该基
因载体的____________上,然后再转移至受体细胞中。将目的基因导入动物细胞的技术
中,应用最多的是_______。
相关文档
- 【英语】四川省棠湖中学2020届高三2021-05-2214页
- 四川省泸县第四中学2020届高三下学2021-05-2216页
- 北京市顺义区牛栏山一中2020届高三2021-05-2224页
- 【英语】湖北省孝感市安陆市第一中2021-05-2219页
- 安徽省六安市第一中学2020届高三下2021-05-2215页
- 【英语】四川省宜宾市叙州区第一中2021-05-2213页
- 四川省宜宾市叙州区第一中学校20202021-05-2218页
- 安徽省六安市第一中学2020届高三下2021-05-2115页
- 2017-2018学年安徽省六安市第一中2021-05-2112页
- 2017-2018学年安徽省六安市第一中2021-05-2116页